Propriedades
Periódicas
Raio atômico – Energia de Ionização – Afinidade Eletrônica – Eletronegatividade – Eletropositividade – Potencial de Ionização
As propriedades periódicas são
tendências ou características que alguns elementos químicos seguem e
que marca sua localização na tabela periódica.
Os elementos químicos são organizados
de acordo com suas propriedades periódicas e tais propriedades são alteradas de
acordo com o número atômico. As principais propriedades periódicas são: Raio
atômico, Energia de Ionização, Afinidade eletrônica, Eletronegatividade,
Eletropositividade e Potencial de Ionização.
Raio atômico
O raio atômico se
refere ao tamanho do átomo. Quanto maior o número de níveis, maior será o
tamanho do átomo. O átomo que possui o maior número de prótons exerce maior
atração sobre seus elétrons.
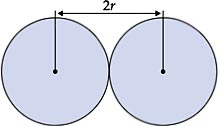
Em outras palavras, raio atômico é a
distância do núcleo de um átomo à sua eletrosfera na camada mais externa.
Porém, como o átomo não é rígido, calcula-se o raio atômico médio pela metade
da distância entre os centros dos núcleos de dois átomos de mesmo elemento numa
ligação química em estado sólido.
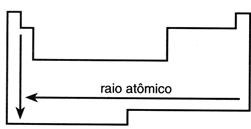
O raio atômico cresce de cima para
baixo na família da tabela periódica, acompanhando o número de camadas dos átomos de cada elemento e da
direita para a esquerda nos períodos da tabela
periódica.
Quanto maior o número atômico de um
elemento no período, maiores são as forças exercidas entre o núcleo e a
eletrosfera, o que resulta num menor raio atômico.
O elemento de maior raio atômico é o
Césio.
Energia de Ionização
Energia de Ionização é a energia necessária para remover um ou mais elétrons de um
átomo isolado no estado gasoso. O tamanho do átomo interfere na sua energia de
ionização. Se o átomo for grande, sua energia de ionização será menor.
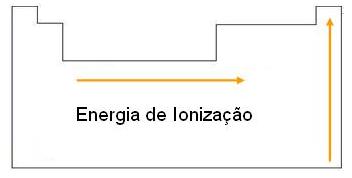
- Em uma mesma família a energia aumenta de baixo para cima;
- Em um mesmo período a Energia de
Ionização aumenta da esquerda para a direita.
Afinidade eletrônica
Afinidade eletrônica é a energia liberada quando um átomo no estado gasoso (isolado)
captura um elétron. Quanto menor o raio, maior a sua afinidade eletrônica, em
uma família ou período.
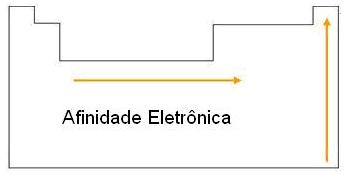
A afinidade eletrônica mede a energia
liberada por um átomo em estado fundamental e no estado gasoso ao receber um
elétron. Trata-se da energia mínima necessária para a retirada de um elétron de
um ânion de um determinado elemento.
Nos gases nobres a afinidade eletrônica não é significativa, porém como
a adição de um elétron em qualquer elemento causa liberação de energia, então a
afinidade eletrônica dos gases nobres não é igual a zero
.
A afinidade eletrônica tem comportamento
parecido com o da eletronegatividade, já que não tem uma forma muito definida
no seu crescimento na tabela periódica: cresce de baixo para cima e da esquerda
para a direita.
O elemento químico que possui a maior
afinidade eletrônica é o Cloro.
Eletronegatividade
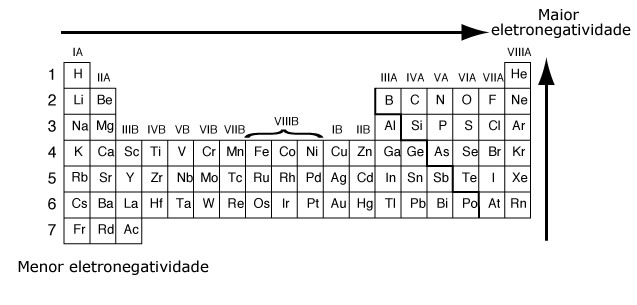
A Eletronegatividade é
a força de atração exercida sobre os elétrons de uma ligação. Na tabela
periódica a eletronegatividade aumenta de baixo para cima e da esquerda para a
direita.
Essa propriedade tem relação com o
raio atômico: quanto menor o tamanho de um átomo, maior é a força de atração
sobre os elétrons.
Segundo a escala de Pauling*, a eletronegatividade cresce na família de baixo para cima, junto com à diminuição do raio atômico e do aumento das interações do núcleo com a eletrosfera e no período da esquerda pela direita, acompanhando o aumento do número atômico.Não é possível calcular a eletronegatividade de um único átomo (isolado), pois a eletronegatividade é a tendência que um átomo tem em receber elétrons em uma ligação covalente. Portanto, é preciso das ligações químicas para medir essa propriedade.
O elemento mais eletronegativo da
tabela periódica é o flúor.
*A escala de Pauling é uma escala
construída empiricamente e muito utilizada na Química. Ela mede a atração que o
átomo exerce sobre elétrons externos em ligações covalentes, ou seja, sua
eletronegatividade.
Eletropositividade
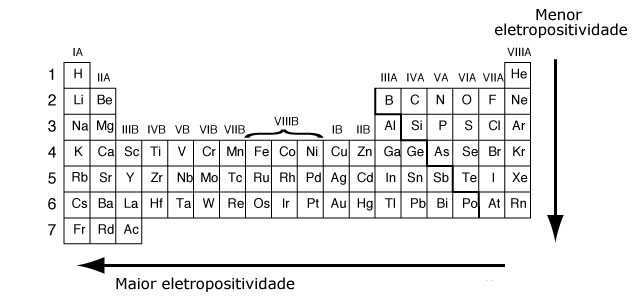
Eletropositividade é a tendência de perder elétrons, apresentada por um átomo. Quanto
maior for seu valor, maior será o caráter metálico. Os átomos com menos de
quatro elétrons de valência, metais em geral, possuem maior tendência em perder
elétrons, por isso, possuem maior eletropositivade. Um aumento no número de
camadas diminui a força de atração do núcleo sobre os elétrons periféricos,
facilitando a perda de elétrons pelo átomo e, consequentemente, aumentando a
sua eletropositividade.
A eletropositividade cresce da
direita para a esquerda nos períodos e de cima para baixo nas famílias.
A forma da medir a eletropositividade
de um elemento é a mesma da eletronegatividade: através das ligação química.
Entretanto, o sentido é o contrário, pois mede a tendência de um átomo em
perder elétrons. Os metais são os mais eletropositivos e os gases nobres são
excluídos¹, pois não têm tendência em perder elétrons.
O elemento químico mais eletropositivo
é o frâncio. Ele tem tendência máxima à oxidação.
¹Como os gases nobres são muito
inertes, os valores de eletronegatividade e eletropositividade não são objetos
de estudo pela dificuldade da obtenção desses dados.
Potencial de Ionização
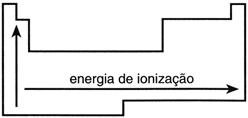
É a energia necessária para remover
um elétron de um átomo isolado no estado gasoso. À medida que aumenta o tamanho
do átomo, aumenta a facilidade para a remoção de um elétron da camada de
valência. Portanto, quanto maior o tamanho do átomo, menor o potencial de
ionização.
O Potencial de Ionização mede
o contrário da afinidade eletrônica: a energia necessária para retirar um
elétron de um átomo neutro, em estado fundamental e no estado gasoso. A
retirada de elétron na primeira vez utilizará uma quantidade de energia maior
que na segunda retirada e assim sucessivamente.
Possui comportamento igual ao da
afinidade eletrônica e da eletronegatividade, portanto, o Flúor e o Cloro são
os elementos que possuem os maiores potenciais de ionização da tabela
periódica.
Nenhum comentário:
Postar um comentário